|
||
 View image in article
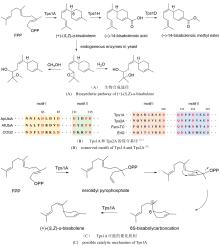
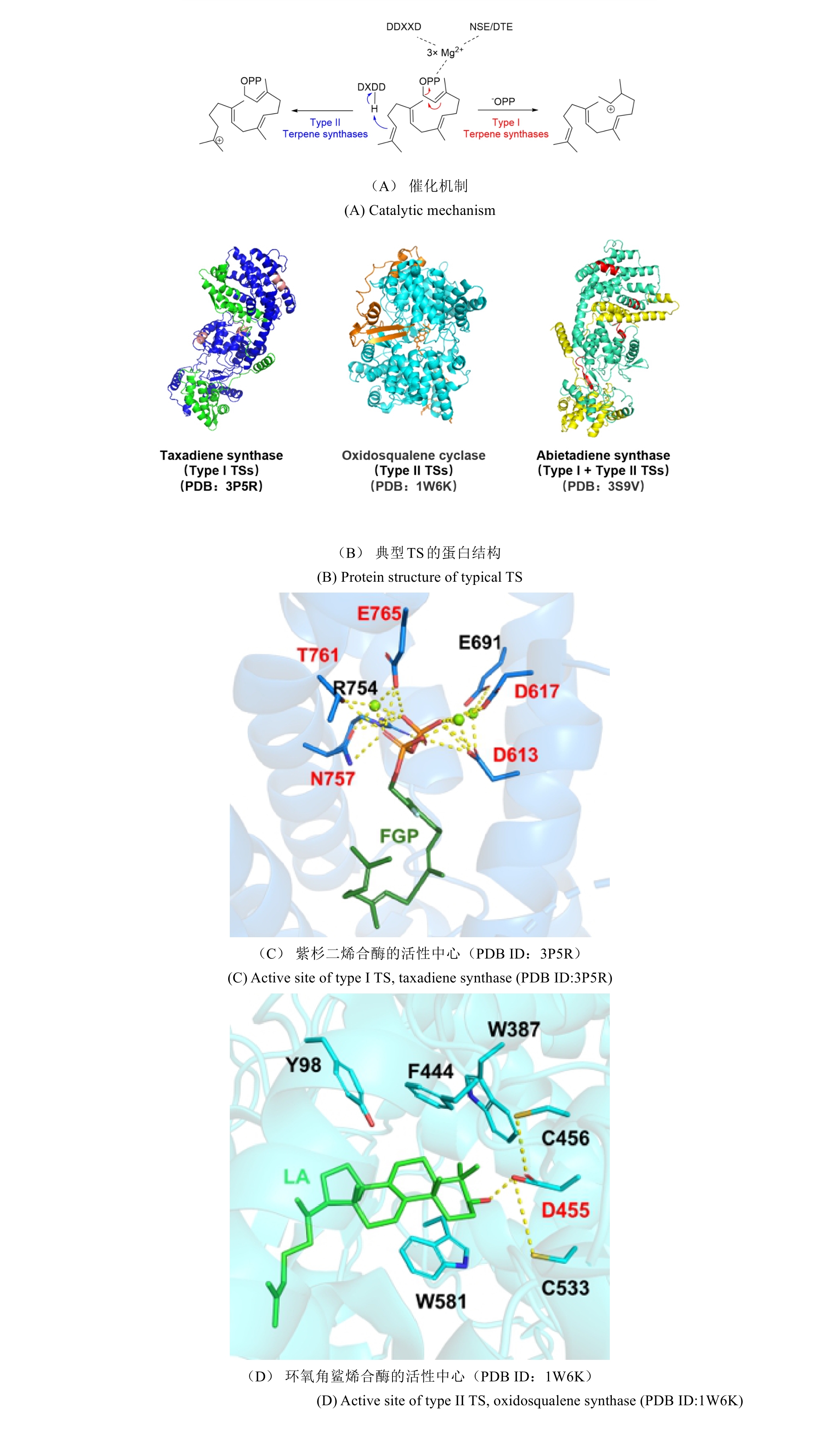
图2
I 型和II型 TS
正文中引用本图/表的段落
通常,萜烯骨架的形成可以经由两种不同的底物激活机制实现(图2)[33-34]:I型TS通过与其保守基序结合的Mg2+促发焦磷酸基团的解离,从而形成碳正离子中间体并引发后续的系列反应;而II类TS则通过其保守基序中的Asp残基诱导底物质子化,从而形成活性中间体起始环化反应。由于绝大多数一致的TSs都可以归类到上述两种类型,因此I型和II 型TS被称为经典的TS。令人振奋的是,随着研究的深入,人们逐渐发现了一些与经典TS截然不同的酶,它们也能通过诱发碳正离子的形成催化类异戊二烯焦磷酸的环化,进而形成结构新颖的萜类化合物。因此,我们称之为非常规的TS,它们在功能上催化类似于经典TS的环化反应,但在序列或结构上却与经典的 TS 迥然不同,其中包含异戊烯基转移酶、甲基转移酶、CYP 和卤代酸脱卤酶等。近年来,得益于测序技术与合成生物学技术的发展,我们进入了快速发现和表征TS和后修饰酶的时期,这些新酶、新元件、新途径的发现又进一步助力了萜类生物合成途径的创新。利用组合生物合成等方式,人们创新性地发现了多种非天然萜类化合物,显著地拓宽了萜类化合物的化学空间。本文综述了近五年在非常规TS和非天然萜类生物合成途径方面取得的最新进展,着重介绍了非常规TS的类型、序列、结构和催化机理(表1),同时也介绍了通过组合MT+TS、CYP+TS等方式合成非天然萜类化合物的研究进展。最后,对萜类生物合成研究的发展趋势进行了展望,以期为未来新型萜类化合物的发现和生物合成提供启示。
TS能够将线性类异戊二烯前体转化为成千上万种环化的萜类化合物。如前所述,典型的TS可以根据其形成碳正离子中间体机制的不同分为I型和II型(图2)。I型TS具有高度保守的DDxxD 和(N/D)xx(S/T)xxxE基序。I型TS通过Mg2+与线性前体的焦磷酸基团结合并诱导其解离,形成高活性的碳正离子中间体,从而引发后续的环化级联反应[45-47]。II型TS通常仅含有DxDD保守基序,它通过基序中的Asp残基将类异戊二烯基焦磷酸前体中的双键质子化,进而形成碳正离子中间体引发后续反应,最后终止于质子的消除反应[48]。I型TS通常参与半萜、单萜、倍半萜以及部分二萜的生物合成,例如Taxus brevifolia来源的紫杉二烯合酶[48]。II型TS主要负责催化二萜和缺少焦磷酸基团的直链三萜前体角鲨烯或环氧角鲨烯的质子化和环化,例如人羊毛甾醇合酶(氧化角鲨烯环化酶,OSC)[49] 和来自Alicyclobacillus acidocaldarius的角鲨烯/霍烯环化酶(SHC)[50]。I型和II型TS催化产物的不同,可能取决于它们的活性位点结构、底物折叠模式和关键残基作用[34, 51-52]。通常情况下,I型和II型TS和PT都是单独存在并行使其功能的,但在一些酶中同时存在两种(TS和PT/TS)活性结构域并具有双功能[53]。目前发现的双功能萜类合酶有:I型TS +II型TS、I型TS+PT、II型TS+PT,例如来自大冷杉的松香二烯合酶是一种双功能二萜环化酶,同时具有Ⅰ型和Ⅱ型TS酶的催化活性[54];双功能酶由于两个活性位点在空间位置上接近,往往具有更高的催化效率[34]。
本文的其它图/表
|