|
||
 View image in article
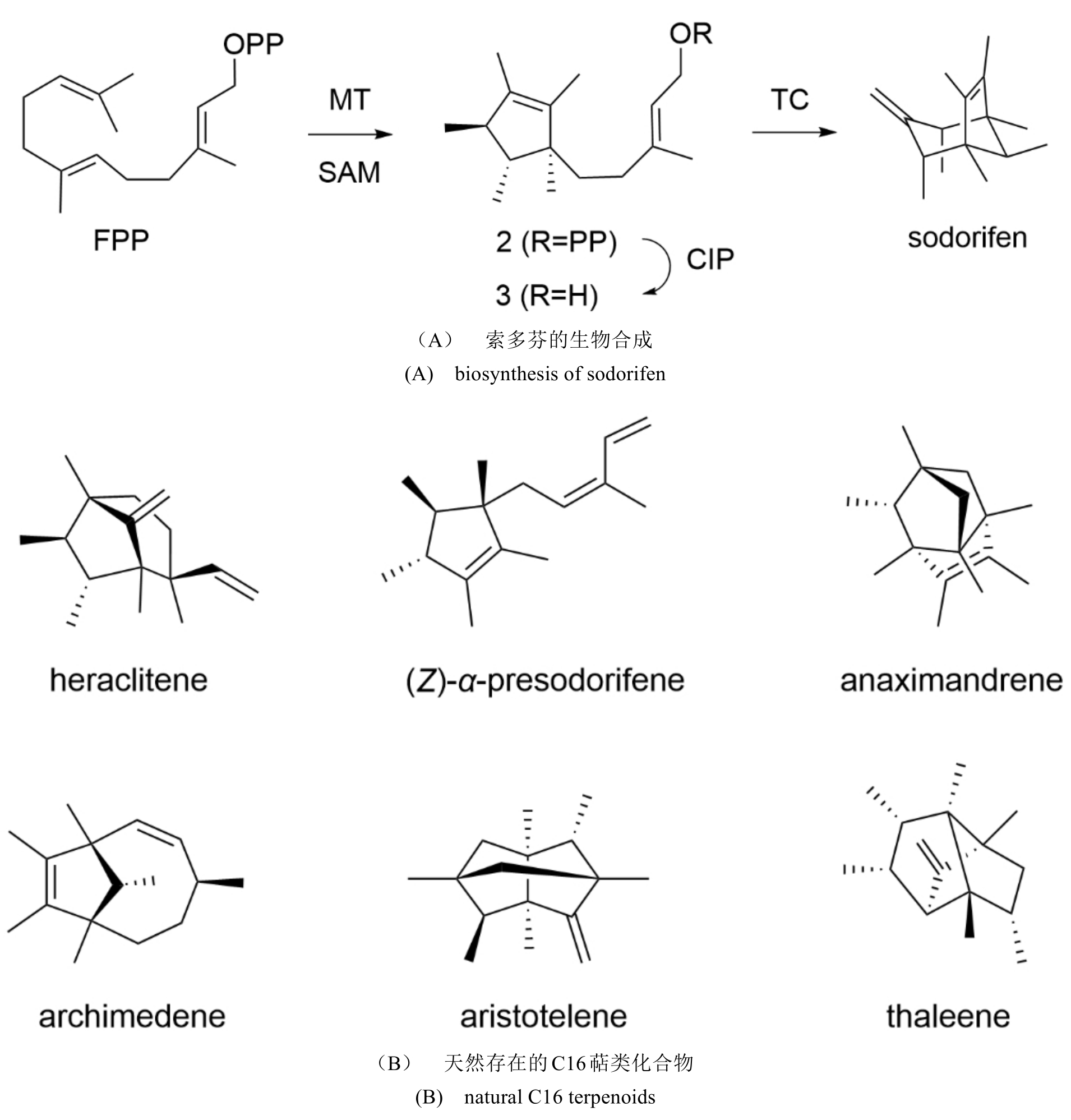
图8
C16萜类化合物
正文中引用本图/表的段落
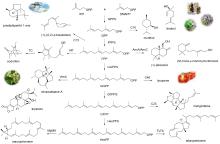
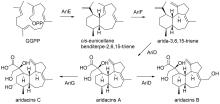
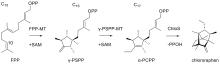
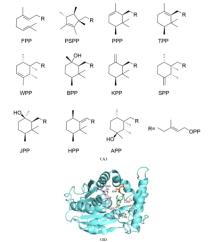
萜类化合物的生物合成以C5异戊二烯结构单元为基础,迄今分离出的几乎所有萜类化合物碳原子数量都是5的倍数[76]。然而,有研究报道在沙雷氏菌(Serratia plymuthica)中发现了一种名为索多芬(sodorifen) 的独特C16萜类化合物[77]。研究人员通过转录组、基因组分析以及敲除实验,找到了S. plymuthica PRI-2C中索多芬合成相关的BGC,有趣的是,索多芬的生物合成仅需要1个SAM依赖型MT(SodC/SpFFPMT)和1个TS(SodD)[78-81]。对其生物合成的进一步研究表明, SodC/SpFFPMT不仅对FPP 的进行甲基化,还表现出环化酶活性,产生单环化合物前索多芬焦磷酸盐(PSPP),SodD则进一步将PSPP环化形成索多芬(图8A)。值得一提的是,SodC/SpFFPMT是第一个已知的不仅催化 FPP 的甲基化,而且还催化萜类环化反应的MT。为了进一步探究其催化机制,研究人员开展了体外酶反应和同位素标记实验[40]。首先利用13C单标记FPP和(甲基-13C)SAM追踪索多芬上所有碳的来源,随后利用13C双/多标记FPP明确相连的碳。进一步,通过合成13C和氘标记底物追踪索多芬上所有氢的来源。结果表明,在酶催化后FPP C4位的pro-S H、C6位的H、C9位的pro-R H分别迁移到了索多芬的C1、C5和C8位,而在终产物索多芬上没有检测到FPP C10位的H。除了上述H,其他所有的H均保留在原位。基于上述同位素追踪结果,研究人员提出了索多芬的生物合成途径。通过TS的催化,PSPP在脱去二磷酸基团后,经历了不同类型的氢迁移、碎片化、[4+3]环加成、碳骨架重排和去质子化反应,最终形成索多芬。
本文的其它图/表
|