|
||
|
Research on live biotherapeutic products in metabolic diseases
Synthetic Biology Journal
DOI: 10.12211/2096-8280.2025-024
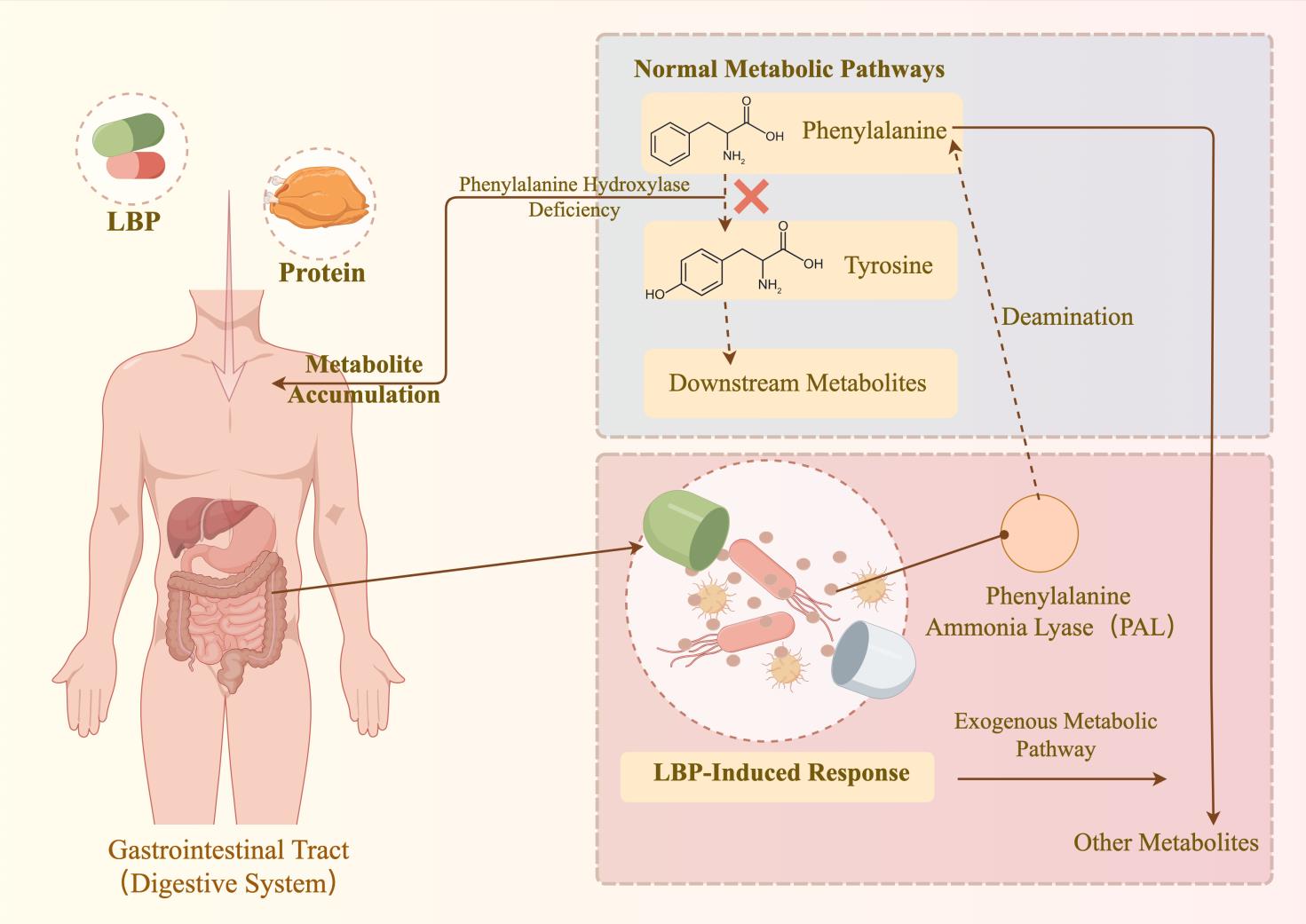
Fig. 1
Pathogenesis of phenylketonuria and corresponding LBP treatment program
Extracts from the Article
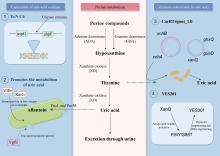
苯丙酮尿症(Phenylketonuria,PKU)是一种相对常见的遗传代谢病,主要由苯丙氨酸羟化酶(Phenylalanine Hydroxylase, PAH)缺陷或功能异常引起,导致苯丙氨酸(Phenylalanine, Phe)在体内积聚(图1)。在正常条件下,苯丙氨酸在PAH的催化作用下转化为酪氨酸。然而,PKU患者因PAH缺陷或完全缺失,致使苯丙氨酸代谢受阻,在体内过量蓄积[8]。高浓度的苯丙氨酸会对中枢神经系统有毒性作用,进而导致智力障碍、癫痫、行为异常及其他神经发育障碍[9]。
针对PKU的病理特点,利用基因工程技术构建LBP已成为一种重要的治疗策略。其核心在于应用基因工程改造的微生物表达特定酶,在肠道内代谢过量的苯丙氨酸,从而降低其异常积累(图1)。例如,Synlogic公司的团队通过基因工程改造E.coli Nissle 1917(EcN)得到菌株SYNB1618[12]。该工程菌株整合了两条降解苯丙氨酸的途径。第一条途径表达苯丙氨酸氨解氨酶(Phenylalanine Ammonia Lyase, PAL),催化苯丙氨酸脱氨为毒性较低的反式肉桂酸(trans-cinnamic acid, TCA)[13]。第二条途径表达L-氨基酸脱氨酶 (L-amino acid deaminase, LAAD),催化苯丙氨酸转化为苯丙酮酸。为实现肠道内苯丙氨酸降解,研究人员在EcN的染色体中整合了基因pheP(编码苯丙氨酸转运蛋白PheP)、基因stlA(编码PAL)和基因pma(编码LAAD),其中2个pheP基因和3个stl1A基因受厌氧诱导型启动子PfnrS控制,1个pma基因由阿拉伯糖诱导型启动子PBAD控制。为保证菌株的生物安全性,研究人员敲除了EcN中的dapA基因,构建了营养缺陷型菌株,使其依赖外源补充的二氨基庚二酸进行细胞壁合成和生长。研究发现,单一提高stlA基因的表达量并不能显著提升全细胞催化活性,因此研究团队致力于提高PAL自身的活性来进一步优化菌株性能。为实现这一目的,研究人员开发了一种TCA的变构转录因子(aTF)生物传感器[14]。利用该生物传感器,研究人员从一个包含超过一百万个变体的PAL突变体库中进行筛选,获得了最高活性突变体mPAL,其酶活性较野生型PAL提高了2倍。基于此,研究人员又构建了菌株SYNB1934。
Other Images/Table from this Article
|