生命科学与工程学、系统科学、信息科学、合成科学的交叉融合,不仅使人类对于生命本质的认知从“格物致知”上升至“建物致知”[1],同时也为健康、资源、环境、工业、农业等领域的重大问题解决提供了新途径。专利文献是记载合成生物学技术发展的重要信息载体,对其的检索、统计、分析可用于揭示合成生物学发展的技术生命周期,透视合成生物学发展的技术脉络,剖析合成生物学领域的竞争格局,启示合成生物学领域的技术发展空间、专利布局空间和知识产权运营策略。本文基于对合成生物学专利的系统性检索和分析,梳理合成生物学的发展态势,以期为合成生物学技术的开发、专利运营等提供决策参考。
1 会聚理念和多元资助,促进合成生物学快速发展
图 1
图 1
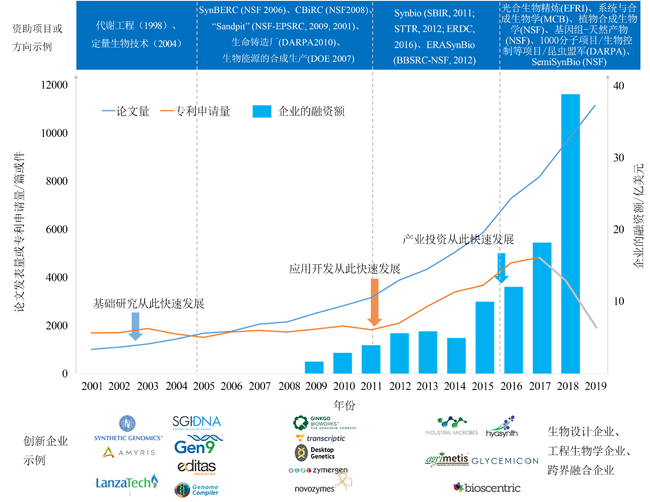
2001—2019年合成生物学的论文、专利和融资和企业发展情况
(1.论文检索的数据库为Web of Science,专利检索的数据库为incoPat,论文和专利的检索范围均为全球文献,论文和专利的检索日期为2020年1月21日;2.企业的融资额数据引用的是SynBioBeta的合成生物学企业融资数据(2009—2018)[3];3.鉴于美国在合成生物学领域总体上处于领先地位,合成生物学资助项目示例以美国国家科学基金会(National Science Foundation,NSF)、美国国防高级研究计划局(Defense Advanced Research Projects Agency,DARPA)等为代表;4.合成生物学创新企业的示例,以对应阶段的典型产品的开发企业为代表;5.由于专利公开滞后等原因,近两年的专利数量仅供参考)
Fig. 1
Papers, patents, financing, and corporate development related to synthetic biology from 2001 to 2009
从2000—2019年的发展历程来看,合成生物学的发展大体经历了4个阶段。第一阶段(2005年以前):以基因线路在代谢工程领域的应用为代表,这一时期的典型成果是青蒿素前体在大肠杆菌中的合成[4]。第二阶段(2005—2011年):基础研究快速发展,年度的专利申请量较之前并未有显著增加,合成生物学研究开发总体上处于工程化理念日渐深入、使能技术平台得到重视、工程方法和工具不断积淀的阶段,体现出“工程生物学”的早期发展特点。第三阶段(2011—2015年):基因组编辑的效率大幅提升,合成生物学技术开发和应用不断拓展,其应用领域从生物基化学品、生物能源扩展至疾病诊断、药物和疫苗开发、作物育种、环境监测等诸多领域。第四阶段(2015年以后):合成生物学的“设计—构建—测试”(Design-Build-Test,DBT)循环扩展至“设计—构建—测试—学习”(Design-Build-Test-Learn,DBTL),“半导体合成生物学”(Semiconductor Synthetic Biology)、“工程生物学”(Engineering Biology)等理念或学科的提出,生物技术与信息技术融合发展的特点愈加明显。
2 合成生物学技术的专利布局和知识图谱
2.1 合成生物学企业的专利布局
经历了上述4个发展阶段后,一批合成生物学企业得以成长,许多以传统化工、医药产品开发为主的企业也将目光投向合成生物学,在元件、基因合成、生物设计、基因编辑技术,以及基因治疗、细胞治疗、疫苗、化学品、生物材料、生物能源、农业和食品等应用领域进行专利布局,开发相关的产品。其中,Agilent Technologies等科学仪器企业较早从事DNA合成仪的开发,而Twist Bioscience等企业则是基于芯片的DNA合成开发的代表(表1)。
表 1 核酸与基因组合成企业的技术或产品其代表性专利(例举)
Tab. 1
| 企业名称 | 国家 (地区) | 成立年份 | 典型技术或产品(在研或已上市) | 代表性专利① (申请号) | 技术内容(及说明) |
|---|---|---|---|---|---|
| Agilent Technologies | 美国 | 1999 (从惠普拆分) | DNA合成仪 | US16/107491 | 寡核苷酸合成的双偶联方法 |
| US13/935201 | 降低合成误差的方法 | ||||
| US09/429054 | 用于寡核苷酸合成的聚合物片材 | ||||
| US09/428332 | 高纯度的寡核苷酸合成 | ||||
| Avecia | 英国 | 1999 | 临床用寡核苷酸 | EP2009734250 | 寡核苷酸(特别是对β-氰乙基保护基)的脱保护 |
| 金斯瑞 | 中国 | 2002 | 重组DNA的克隆 | CN200980143524.3 | 供体DNA分子克隆至受体载体预定位置 |
| Synthetic Genomics | 美国 | 2005 | 合成基因组 | US12/371543 | 体外连接和组合装配核酸分子 |
| Ginkgo Bioworks | 美国 | 2009 | DNA合成与组装 | US15/440293 | 在微阵列平台上原位合成的短寡核苷酸并组装 |
| Synthego | 美国 | 2012 | 合成RNA | US16/027982 | 生物聚合物合成的自动化模块化系统 |
| 泓迅科技 | 中国 | 2013 | 基因合成 | CN201510744597.5 | 核苷酸的芯片高通量合成,DNA的组装 |
| Twist Bioscience | 美国 | 2013 | DNA合成 | US14/452429 | 从头合成的基因文库 |
| Molecular Assemblies | 美国 | 2013 | 核酸合成设备 | CA2958581 | 在不使用核酸模板下从头合成碱基 |
| Nuclera Nucleics | 英国 | 2013 | DNA合成 | GB2015003534 | 用3'-O-偶氮二甲基核苷三磷酸制备核酸 |
| SGI-DNA | 美国 | 2014 | DNA拼装 | US15/667515 | 核酸分子的合成或拼装错误的校正 |
| DNA Script | 法国 | 2014 | 合成DNA | FR2016050804 | 酶促合成长核酸 |
| Evonetix | 英国 | 2015 | 核酸合成 | GB2018001182 | 在固体表面上高保真合成寡核苷酸 (DNA或XNA) |
| Catalog Technologies | 美国 | 2016 | 基于核酸的存储 | PCT/US2017/062098 | 将信息写入核酸序列 |
① 专利族以其中的任一专利号代表。
元件的标准化开发是合成生物学发展的基础,Pivot Bio等企业已经在模块化的DNA分子开发等方面作了布局,而Synthorx在非天然核苷酸技术方面的发展也已受到业界的广泛关注。在底盘细胞、设计工具和基因编辑工具方面,美国、英国等国家(地区)的企业已经开始了较为系统的专利布局(表2)。
表 2 合成生物学元件、底盘细胞、设计工具和基因编辑企业的技术或产品及其代表性专利(例举)
Tab. 2
| 项目 | 企业名称 | 国家 (地区) | 成立 年份 | 典型技术或产品 (在研或已上市) | 代表性专利① (申请号) | 技术内容(及说明) |
|---|---|---|---|---|---|---|
| 元件 | ATG Biosynthetics | 德国 | 2001 | TOGGLE Assembly 载体系统 | DE102013006487 | 基于合成DNA的功能元件的替换系统 |
| Atum | 美国 | 2003 | 基于GeneGPS®和VectorGPS®的 DNA2.0 | PCT/US2018/045041 | DNA载体和真核细胞表达元件 | |
| PCT/US2017/040991 | 体外应用的DNA聚合酶序列及其修饰 | |||||
| Horizon Discovery Group | 英国 | 2005 | 转座子系统 | GB2016002473 | 侧接“复制和粘贴”转座子末端序列 | |
| Pivot Bio | 美国 | 2010 | 模块化的DNA分子 | US13/939110 | 组装两种或更多种DNA分子的方法 | |
| Enevolv | 美国 | 2011 | 无细胞传感器 | PCT/US2017/047009 | 与目标分子结合的变构DNA结合蛋白传感器,由工程化的原核转录调节子家族成员组成 | |
| Oxford Genetics | 英国 | 2011 | DNA质粒系统 | GB2011019987 | 允许在质粒载体内交换启动子的基因工程平台 | |
| Synthorx | 美国 | 2014 | 非天然核苷酸 | US16/530742 | 插入利用突变体tRNA的非天然氨基酸的方法 | |
| 底盘细胞 | Biogen | 美国 | 1978 | 外源分子的表达盒 | US10/545420 | 驱动真核宿主细胞转录的包括启动子、增强子、插入区、聚腺苷酸化信号结构域 |
| Scarab Genomics | 美国 | 2002 | Clean Genome® | US10/655914 | 显著减少基因组大小的特异性大肠杆菌菌株 | |
| B-Mogen Biotechnologies | 美国 | 2015 | 定制细胞设计 | US15/958834 | TcBuster转座酶和转座子 | |
| 生物设计 工具 | Biomax Informatics | 德国 | 1997 | Pedant-Pro ™ 序列分析套件 | DE10205091 | 无细胞表达系统的表达效率预测方法 |
| Arzeda | 美国 | 2008 | Scylax™ (酶设计) | US16/008924 | 酶的配体结合和催化活性等特性的计算和设计 | |
| US14/214571 | C5材料(乙酰丙酸等)合成的设计 | |||||
| Synpromics | 英国 | 2010 | PromPT™ | EP2012704725 | 数据驱动的启动子设计 | |
| Synthace | 英国 | 2011 | 生物过程设计软件 | GB2014005246 | 根据标准化元件结构(含导入、参数、数据、物理输入、要求、设置等功能区块)定义单元操作 | |
| Transcriptic | 美国 | 2012 | 远程实验室系统 | US14/629371 | 实验室自动化与通用语言 | |
| Dovetail Genomics | 美国 | 2013 | Dovetail™ 基因组注释 | US16/078741 | 序列数据(如基因组序列数据)的准确定相读取 | |
| 基因编辑 | Sigma Aldrich | 美国 | 1975 | 基因组编辑工具 | US15/188902 | 工程化RNA介导的核酸内切酶复合物 |
| Toolgen | 韩国 | 1999 | 基因编辑工具 | KR1020177003312 | RNA引导的工程核酸酶 | |
| Precision Biosciences | 美国 | 2006 | 治疗用基因组 编辑的平台 | PCT/US2008/085878 | 非天然存在的大范围核酸酶(具有改变的DNA识别序列特异性和/或改变的亲和力) | |
| Caribou Biosciences | 美国 | 2011 | 基因组编辑工具 | US14/997467 | Ⅱ型CRISPR-Cas9-缔合的分裂-连接多核苷酸组合物 | |
| Intellia Therapeutics | 美国 | 2014 | 用于免疫肿瘤学的 基因组编辑系统 | US15/780751 | 含tracr和crRNA的gRNA分子 | |
| Poseida Therapeutics | 美国 | 2015 | 治疗用的基因组 编辑工具 | US15/199021 | 聚合物囊泡中的基因编辑系统 | |
| Inscripta | 美国 | 2015 | 数字化的基因组 编辑工具 | US16/357443 | 产生嵌合核酸酶核酸序列文库的方法 | |
| Arbor Biotechnologies | 美国 | 2016 | 超高通量蛋白 | US15/916271 | 工程改造的CRISPR系统和组件 | |
| Beam Therapeutics | 英国 | 2017 | 遗传疾病的治疗 | PCT/US2019/031899 | 可编程的碱基编辑器 |
①专利族以其中的任一专利号代表。
在疫苗开发、基因治疗、细胞治疗、治疗用微生物开发等医学领域,合成生物学的应用前景广阔。Sarepta Therapeutics等成立较早的企业,在21世纪初已将目光投向了合成生物学,而2010以来更是有一大批致力于治疗应用的合成生物学企业得以创立(表3)。
表 3 合成生物学在疫苗和治疗领域应用的企业技术或产品及其代表性专利(例举)
Tab. 3
| 应用领域 | 企业名称 | 国家 (地区) | 成立 年份 | 典型技术或产品 (在研或已上市) | 代表性专利 (申请号) | 技术内容(及说明) |
|---|---|---|---|---|---|---|
| 基因治疗 和细胞治疗 | Sarepta Therapeutics | 美国 | 1980 | 基因治疗 | US15/293961 | 反义核苷酸 |
| Sangamo Therapeutics | 美国 | 1995 | 遗传病的基因治疗 | US14/939719 | 优化的锌指蛋白 | |
| Oxford Biomedica | 英国 | 1995 | 基因和细胞治疗 | GB2011018636 | 包含多巴胺合成酶酪氨酸羟化酶、GTP-环化水解酶I、芳香族氨基酸多巴脱羧酶的构建体 | |
| Cellectis | 法国 | 1999 | 基因编辑的工程化 免疫细胞 | US12/091216 | 由可移动遗传元件编码的核酸内切酶 | |
| US15/118801 | 抗原标记的表达或递呈的免疫细胞基因编辑 | |||||
| 宝生物 | 日本 | 2002 | 基因治疗用的载体 | JP2009511821 | 产生逆转录病毒载体的细胞 | |
| 基因治疗 和细胞治疗 | Casebia Therapeutics | 美国 | 2011 | 血友病治疗 | US16/163536 | 敲除基因组中的FVⅢ编码基因(用基因编辑) |
| 色素性视网膜炎 的治疗 | US16/198361 | 针对常染色体显性视网膜色素变性,编辑RHO基因 | ||||
| 新型RNA可编程 核酸内切酶系统 | PCT/US2018/065863 | 来自金黄色葡萄球菌(SluCas9)的CRISPR-Cas9家族的新型CRISPR-Cas内切核酸酶及其变体 | ||||
| Phio Pharmaceuticals | 美国 | 2011 | RNAi药物 | US12/867181 | 具有19~49个核苷酸的双链区域 | |
| Translate Bio | 美国 | 2011 | MRTTM(mRNA治疗平台) | US14/775844 | 在5'末端加适当的帽,保护mRNA免于降解并促进成功的蛋白质翻译 | |
| Homology Medicines | 美国 | 2012 | β-地中海贫血治疗 | US16/163061 | β珠蛋白基因(HBB)基因突变的腺相关病毒(AAV) | |
| Bluebird Bio | 美国 | 2012 | ZYNTEGLO™ (β-地中海贫血治疗) | PCT/US2017/017372 | 用于基因治疗的增强子组合物 | |
| Abeona Therapeutics | 美国 | 2013 | ABO-101和ABO-102(孤儿药) | US13/491326 US14/950387 | 基于腺相关病毒(AAV)载体的圣菲利波综合征的基因治疗(从美国儿童医院获得专利许可) | |
| ABO-201和ABO-202(孤儿药) | US62/092501 US62/146793 | 基于腺相关病毒载体的巴顿病的基因治疗(从UNeMed公司获得专利许可) | ||||
| EB-101(孤儿药) | US13/472260US13/594773 US13/297110 US12/538791US11/731314 | 产生重组AAV衣壳文库的方法、用于核酸转移的嵌合AAV衣壳蛋白,可用于疱性表皮松解症的治疗(从斯坦福大学获得专利许可) | ||||
| AIM™衣壳文库 | US15/525214 | 靶向中枢神经系统的嵌合AAV衣壳(从北卡罗来纳大学获得专利许可) | ||||
| Arcturus Therapeutics | 美国 | 2013 | LUNAR®递送系统, 用于鸟氨酸氨甲酰转 移酶缺乏症、囊性纤维 化等治疗 | US14/703016 | 羟甲基取代的核苷酸单体 | |
| US15/393840 | 脂质体递送系统 | |||||
| US15/272107 | 用于引导基因编辑的导向分子 | |||||
| Crispr Therapeutics | 瑞士 | 2013 | 严重联合免疫缺陷 的治疗 | US16/074743 | 编辑重组激活基因1(RAG1)基因 | |
| 杜氏肌营养不良症 的治疗 | US15/763328 | 在诱导性多能干细胞(iPSC)的肌营养不良蛋白基因内或附近编辑 | ||||
| Editas Medicine | 美国 | 2013 | β血红蛋白病 | PCT/US2017/022377 | 用基因组编辑系统增加γ-珠蛋白基因表达 | |
| 博雅辑因 | 中国 | 2015 | ET-02(通用型嵌合 抗原受体T细胞) | CN201811088292.3 | 通过CRISPR/Cas9基因编辑技术同时敲除T细胞的TCR和/或HLA和/或PD‑1蛋白 | |
| Senti Biosciences | 美国 | 2016 | 获得性免疫治疗 | PCT/US2018/022855 | 免疫调节的细胞线路 | |
| 疫苗 | Vertex Pharmaceuticals | 美国 | 1989 | 流感疫苗 | US15/475237 | 流感A病毒变体 |
| Inovio Pharmaceuticals | 美国 | 1979 | 流感疫苗 | US12/269824 | 启动子连接到编码调节抗原表达的抗原核酸序列 | |
| Glaxosmithkline | 英国 | 2000(合并而成) | 艰难梭菌防治用 的疫苗 | EP2012726374 | 免疫原性片段的融合蛋白 | |
| Codagenix | 美国 | 2012 | 减毒活疫苗 | PCT/US2017/053047 | 使用软件重新编码病毒的基因组 | |
| Vir Biotechnology | 美国 | 2016 | HIV疫苗 | IN201737014998 | 使用EpiGraph方法产生的抗原氨基酸序列 | |
| Microsynbiotix | 爱尔兰 | 2016 | 动物疫苗 | US16/092279 | 重组序列和启动子连接的序列 | |
| 治疗用 微生物 | Bioneer | 韩国 | 1992 | 乳酸菌产胞外多糖 | US12/376368 | 加氏菌素BNR17基因的重组载体 |
| Oragenics | 美国 | 1996 | 口腔微生物组 | PCT/US2011/020826 | 非复制型微生物 | |
| Intrexon | 美国 | 1998 | 治疗用活细菌 | US12/522527 | 衍生自乳球菌的序列作为启动子 | |
| Synthetic Biologics | 美国 | 2001 | β-内酰胺酶制剂 | US14/878155 | β-内酰胺酶或其变体或片段作为功能元件 | |
| Prokarium Holdings | 英国 | 2007 | 口腔活细菌递送 | US13/143829 | 表达细胞因子的生物线路 | |
| Vedanta Biosciences | 美国 | 2013 | 微生物组免疫治疗 | PCT/US2017/037498 | 针对难辨梭菌感染的遗传改造的微生物组 | |
| Azitra | 美国 | 2014 | 皮肤病的重组微生 物治疗 | US16/010051 | 表达重组LEKTI结构域的工程化微生物 | |
| US15/312441 | 产生重组聚丝蛋白的工程菌株 | |||||
| Chain Biotechnology | 英国 | 2014 | 梭菌辅助药物开 发(CADD™)平台 | GB2018004548 | 产D-β-羟基丁酸酯的益生菌 | |
| Eligo Bioscience | 法国 | 2014 | 克服病原体耐药性 的广谱噬菌粒疗法 | EP2017305126 | 含正调控的大肠埃希氏杆菌启动子等元件 | |
| Novome Biotechnologies | 美国 | 2015 | 工程化的活细菌 | PCT/US2017/066408 | 遗传修饰的细菌细胞的肠道定植 | |
| Locus Biosciences | 美国 | 2015 | 噬菌体组合物 | US15/777615 | 用CRISPR-Cpf1系统杀死靶细菌 | |
| Biomx | 美国 | 2017 | 噬菌体疗法 | PCT/IB2018/001128 | 裂解克雷伯氏菌属细菌的噬菌体(炎性肠病调节) | |
| PCT/US2018/063842 | 裂解痤疮丙酸杆菌的噬菌体(炎性肠病调节) |
除直接应用于疫苗和治疗领域外,合成生物学在医用蛋白的生产或医学研发中或也发挥重要作用,因而Bristol-Myers Squibb、Gilead Sciences、Astrazeneca也已将目光投向合成生物学。此外,合成生物学在生物基化学品的合成、生物材料、生物能源、现代农业、环境治理等领域也有着广泛的应用前景(表4)。
表 4 合成生物学在其他领域应用企业的技术或产品及其代表性专利(例举)
Tab. 4
| 应用领域 | 企业名称 | 国家 (地区) | 成立 年份 | 典型技术或产品 (在研或已上市) | 代表性专利① (申请号) | 技术内容(及说明) |
|---|---|---|---|---|---|---|
| 蛋白质 和多肽 | Bristol-Myers Squibb | 美国 | 1887 | 蛋白表达操纵系统 | US15/774138 | 操纵和/或控制多肽的蛋白质品质 |
| Gilead Sciences | 美国 | 1987 | MMP9结合蛋白 | US13/935370 | 编码结合基质金属蛋白酶-9(MMP9)的细胞 | |
| Astrazeneca | 英国 | 1999(合并而来) | γ-羧化的蛋白质 | US13/665441 | 表达需要γ-羧化的重组蛋白、维生素K环氧化还原酶和γ-谷氨酰羧化酶的细胞 | |
| Codexis | 美国 | 2002 | CodeEvolver®平台 (蛋白质筛选生产) | US14/768408 | 编码工程化转氨酶多肽的多核苷酸 | |
| US12/483089 | 合成、克隆、转化和筛选多核苷酸变体的大型多样文库的方法 | |||||
| Ambrx | 美国 | 2003 | 非天然多肽 | US11/924101 | 正交氨酰基tRNA合成酶(O-RS) | |
| Spiber | 日本 | 2007 | 蜘蛛丝 | JP2008548463 | 表达大壶腹腺蛛丝蛋白的基因线路 | |
| Azargen Biotechnologies | 南非 | 2009 | 肺表面活性蛋白 | IL242708 | 用植物细胞表达肺表面活性蛋白 | |
| EP2015724025 | 合成启动子 | |||||
| Bolt Threads | 美国 | 2009 | MICROSILK ™ (蜘蛛纤维) | US15/558548 | 具有长精确重复单元的长多肽的基因 | |
| B-SILK ™(丝蛋白) | US15/920331 | 高分泌产量的重组蛋白 | ||||
| Geltor | 美国 | 2015 | 胶原蛋白 | PCT/US2018/061882 | 利用机器学习设计胶原多肽的非天然合成方案 | |
| 化学品、生物材料及生物能源 | Bayer | 德国 | 1863 | 类固醇 | US10/355238 | 3-酮类固醇-Δ1-脱氢酶的过表达 |
| BASF | 德国 | 1865 | 琥珀酸 | EP2010708150 | 下调的内源性PFL酶活性的工程菌 | |
| Cargill | 美国 | 1865 | 醛缩酶催化的产品 | US13/235107 | 编码具有醛缩酶活性多肽的多核苷酸的制备 | |
| Dupont | 美国 | 1897 | 二十碳五烯酸 | US11/264737 | 含油酵母解脂耶氏酵母的工程化菌株 | |
| Goodyear Tire & Rubber | 美国 | 1898 | 异戊二烯聚合物 | US12/459399 | 与启动子连接并编码异戊二烯合酶多肽的线路 | |
| DSM | 荷兰 | 1902 | 多烯脂肪酸 | EP2010178911 | 破囊壶菌表达系统的启动子 | |
| Corbion | 荷兰 | 1919 | 油脂化学品 | US13/630757 | 含脂酶、蔗糖转运蛋白、蔗糖转化酶、果糖激酶、多糖降解酶、酮酰基‑ACP合酶、脂肪酰基‑ACP硫酯酶、脂肪酰基‑辅酶A/醛还原酶、脂肪酰基‑辅酶A还原酶、脂肪醛还原酶、脂肪醛脱羰基酶和/或酰基载体蛋白对应基因的生物线路 | |
| Roquette Freres | 法国 | 1933 | 花生四烯酸 | FR2012057691 | 合成花生四烯酸的高山被孢霉的基因线路 | |
| 钟渊化学 | 日本 | 1949 | 聚羟基链烷酸酯 | JP2007542665 | 硫解酶基因、还原酶基因、聚羟基丁酸合酶基因、聚羟基链烷酸酯合酶基因等组成的生物线路 | |
| Yield10 Biosciences | 美国 | 1992 | 多羟基丁酸酯 | US12/764516 | 将多个基因导入植物,使其产聚羟基链烷酸酯 | |
| Genomatica | 美国 | 1998 | 1,4-丁二醇 | US13/286135 | 4‑羟基丁酸和1,4‑丁二醇的生物合成途径 | |
| Phytowelt Green Technologies | 德国 | 1998 | α-紫罗兰酮 | EP2015757235 | 编码番茄红素ε-环化酶(EC)的序列、编码α-紫罗兰酮生物合成组分等组成的生物线路 | |
| Exxonmobil | 美国 | 1999(合并而来) | 脂肪酸 | US13/453235 | 表达脱氢酶以合成脂肪酸、脂肪酸衍生物或脂质 | |
| Novozymes | 丹麦 | 2000 | 生物质降解酶 | DK2011701416T | 编码α‑淀粉酶的多核苷酸 | |
| Modular Genetics | 美国 | 2000 | 酰基氨基酸 | US14/776805 | 工程改造的肽合成酶多肽的基因线路 | |
| Glycosyn | 美国 | 2002 | 岩藻糖基化低聚糖 | US15/307914 | α(1,2)岩藻糖转移酶的表达线路 | |
| Green Biologics | 英国 | 2002 | 3‑羟基丙醛 | GB2014014737 | 含甘油二醇脱水酶的生物线路 | |
| Amyris | 美国 | 2003 | 青蒿素 | US11/419975 | 青蒿素前体的微生物合成 | |
| 生物橡胶 | US14/062798 | 甲羟戊酸(MEV)途径合成异戊二烯 | ||||
| 萜类化合物 | US13/542491 | 萜烯合酶变体的宿主细胞 | ||||
| Evolva | 瑞士 | 2004 | 白藜芦醇 | DK2006708430T | 合成白藜芦醇的生物线路 | |
| 藏红花化合物 | EP2012768896 | 合成藏红花化合物的生物线路 | ||||
| 罗汉果化合物 | EP2012819015 | 合成罗汉果化合物的生物线路 | ||||
| 赤松素 | EP2007787741 | 合成赤松素的生物线路 | ||||
| Aemetis | 美国 | 2005 | 乙醇 | US12/112776 | 降解植物的海洋细菌(Saccharophagus degradans)的纤维素酶和辅助酶、酶混合物 | |
| Gevo | 美国 | 2005 | 异丁醇 | PCT/US2013/041064 | 表达转运蛋白的重组酵母 | |
| Lanzatech | 新西兰 | 2005 | 生物能源 | NZ584652 | 以一氧化碳为底物产乙醇的生物线路 | |
| Global Bioenergies | 法国 | 2008 | 烯烃 | US15/101148 | 将3-羟基羧酸经酶促转化为3-羟基羧基-核苷酸的生物途径 | |
| Lygos | 美国 | 2010 | L‑天冬氨酸 | CA3042854 | 编码L-天冬氨酸途径酶和L-天冬氨酸1-脱羧酶 | |
| Nucelis | 美国 | 2010 | 角鲨烯 | US12/471273 | 乙酰辅酶A羧化酶和HMG-CoA还原酶组成的线路 | |
| Silicolife | 葡萄牙 | 2010 | 正丁醇 | PCT/EP2019/057944 | 表达2-羟基戊二酸脱氢酶,谷氨酸-CoA转移酶,戊二酰辅酶A-脱氢酶等的基因线路 | |
| Calysta | 美国 | 2012 | FeedKind®(用天然气制蛋白 质或其他化合物) | US15/311080 | 以天然气或甲烷为原料,利用重组C1代谢微生物,制备脂肪酰‑辅酶A、脂肪醛、脂肪醇、脂肪酯蜡、烷类和酮类等极长碳链化合物(长于C24) | |
| Biosyntia | 丹麦 | 2012 | 维生素B1 | EP2016822958 | 合成硫胺素的大肠埃希氏菌细胞工厂 | |
| Versalis | 意大利 | 2012 | 纤维素的降解 | US15/361732 | 含淀粉水解酶等元件 | |
| Zymergen | 美国 | 2013 | 工业菌株 | US16/313613 | 葡萄糖通透酶基因,及其受天然谷氨酸棒杆菌启动子或由其衍生的突变启动子控制的表达线路 | |
| Zymochem | 美国 | 2013 | 生物基化学品 | IN201627009507 | 表达己二酸途径酶,6-氨基己酸途径酶,ε-己内酰胺途径酶,6-羟基己酸途径酶等的基因线路 | |
| Antheia | 美国 | 2013 | 生物碱 | US16/149025 | 工程化的差向异构酶 | |
| String Bio | 印度 | 2013 | 琥珀酸 | IN1910CHE2014 | 以有机废物/生物气/甲烷为原料生产的微生物 | |
| Industrial Microbes | 美国 | 2013 | 以甲烷为原料的化合物制造系统 | US15/777158 | 可溶性甲烷单加氧酶系统 | |
| 20N Labs | 美国 | 2013 | 有机物合成的开源平台 | US15/408319 | 生物合成对乙酰氨基酚、对氨基酚和对氨基苯甲酸 | |
| US15/408317 | 肌肽和β-丙氨酸的生物合成 | |||||
| Colorifix | 英国 | 2016 | 微生物染色织物 | US15/564713 | 合成色素的生物线路 | |
| Lumen Bioscience | 美国 | 2017 | 甘油三酯 | US13/761025 | 编码二酰甘油酰基转移酶等的蓝细菌基因线路 | |
| 农业 | KWS SAAT SE | 德国 | 1856 | 植物育种 | DE102006029129 | 病原体-诱导合成启动子 |
| 先正达/中化 | 瑞士/中国 | 2000(合并而来)/2019 | 植物调节序列 | EP2009798436 | 将目标的编码蛋白的多核苷酸的表达导向非花粉组织(不导向花粉组织) | |
| Cibus | 美国 | 2001 | RTDS™ (植物育种) | US14/777410 | 寡核苷酸介导的基因修复,提高靶向基因修饰效率 | |
| Arcadia Biosciences | 美国 | 2002 | 高γ-亚麻酸红花 | US13/025345 | γ-亚麻酸的生物合成途径 | |
| 高效氮源利用的 单子叶植物 | US11/644321 | 通过遗传构造修饰以增加丙氨酸转氨酶表达水平 | ||||
| Agrivida | 美国 | 2003 | 用于畜牧营养的GRAINZYME® | US14/433104 US14/433113 | 内含肽修饰的蛋白酶 | |
| Recombinetics | 美国 | 2008 | 基因编辑的动物 | US14/698561 | 利用靶向性核酸酶和同源性定向修复(HDR)的编辑 | |
| Benson Hill Biosystems | 美国 | 2012 | CropOS™作物设计 | US15/324501 | 转录因子(TF)的表达 | |
| Agrimetis | 美国 | 2014 | L‑草胺膦 | US15/445254 | D-氨基酸氧化酶(DAAO)酶、转氨酶(TA)等 | |
| G+Flas Life Sciences | 韩国 | 2014 | 植物表达系统 | KR1020197036068 | 使用CRISPR系统的植物基因组缺失和替换方法 | |
| Egenesis | 美国 | 2015 | 可移植猪器官 | PCT/US2018/028539 | 产生猪内源性逆转录病毒(PERV)元件的多重遗传修饰动物的方法 | |
| Tropic Biosciences UK | 英国 | 2016 | 热带作物改造 | GB2017008662 | 香蕉树的基因组编辑 | |
| 食品 | 味之素 | 日本 | 1909 | L-氨基酸 | JP2005021722 | ybjE基因的增强表达 |
| L-谷氨酸 | JP2012134820 | yggB基因的表达调控 | ||||
| L-赖氨酸和L-苏氨酸 | JP2004222088 | 埃希氏菌的生物线路 | ||||
| C-Lecta | 德国 | 2004 | 海藻糖 | US16/335987 | 热稳定的海藻糖磷酸化酶 | |
| Ardra Bio | 加拿大 | 2016 | 香料 | US16/225611 | 用醛缩酶制反式-2-不饱和醛、δ-内酯和γ-内酯 | |
| Biocapital | 美国 | 2016 | 甜菊糖苷 | PCT/US2018/050143 | 合成甜菊糖苷的生物线路 | |
| 类胡萝卜素 | PCT/US2017/058940 | 合成类胡萝卜素的生物线路 | ||||
| Impossible Foods | 美国 | 2011 | 人造肉 | US15/678891 | 转录激活因子与甲醇诱导型启动子元件连接 | |
| 环境和 卫生检测 | Sample6 Technologies | 美国 | 2009 | 李斯特菌检测 | US14/309389 | 编码标记物的重组噬菌体 |
①专利族以其中的任一专利号代表。
2.2 合成生物学技术的知识图谱
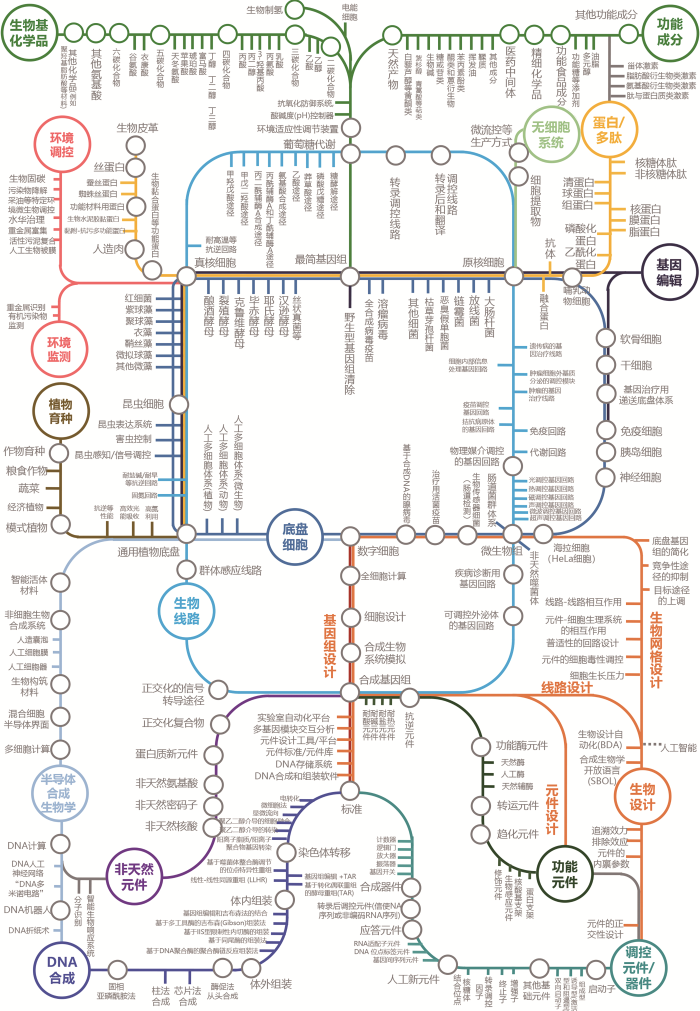
在合成生物学领域的专利权人中,除企业专利权人外,高校、研究机构布局了较多的专利。本文通过以下方法对合成生物学技术的发展进行系统梳理,绘制了合成生物学技术知识图谱(图2):首先,通过对合成生物学代表性企业的专利技术进行解析、梳理、归纳,总结其关键的技术主题或技术内容。其次,针对这一主题的技术内容,对专利进行扩展检索,总结凝练同一技术主题下所涉的其他相关技术内容。再次,根据技术主题间的关联、同一发明人或同一专利权人的技术关联、专利间引证关系,通过知识图谱的形式描绘合成生物学专利的技术内容关系。最后,基于非专利信息的检索,对合成生物学技术的知识图谱进行了补充完善。
图 2
基于专利分析的知识图谱的绘制,目的在于减少交互过程中的“信息不对称”、构建适于合成生物学技术发展的“知识‘底盘’” 贯穿技术发展和转化应用的整个价值链。图谱绘制的基本思路是,将单个专利所对应的技术点设想为基本的“元件”,多个相关“元件”构成 “模块”,不同“模块”的组合体构成 “线路”,若干“线路”的专利或可构成专利池。
在合成生物学技术的知识体系中,DNA合成技术的发展、合成生物学元件的开发是基础。其中,合成生物学元件根据来源可分为天然元件和非天然元件,根据作用又可分为调控元件和功能元件等。立足元件的标准化开发,利用生物设计的工具,已有诸多的专利权人将其开发成各类生物线路。这些生物线路在底盘细胞或无细胞系统中,用于生物基化学品、功能成分、蛋白质或多肽的表达,以及环境调控和监测、植物育种等领域的应用。
3 总结与展望
2011年以来,全球合成生物学技术的专利布局进入加速期,相关专利的申请量快速增长。分析挖掘这些专利中涉及的合成生物学元件、器件、线路和底盘细胞等研发信息及价值,可帮助相关技术的开发和应用,明晰会聚技术体系中各方的定位和作用,也利于打通基础研究到成果转化的各环节,加速产学研协同发展:第一,在研发布局上,通过把握领域发展态势,明确细分方向;第二,在研发过程中,通过对比分析已有技术方案和技术能力的优势和不足,为完善研发及合作策略提供支撑;第三,在技术转化和市场开发时,对比同一主题中的已有专利,可优化专利申请方案,评估界定合成生物学专利价值,为技术许可、转让,以及企业并购、重组、市场定价等提供依据。为进一步促进合成生物学的技术突破和产业发展,提出以下思考和建议。
3.1 推动跨领域的交叉融合,促进使能技术平台和工具的开发
DNA合成、生物线路设计等使能技术和工具是合成生物学技术体系中的基础和关键。尽管不少专利并未将其作为主权利要求加以保护,但在从属权利要求或专利实施例中却清晰可见这些技术或工具的重要性。为准确、定量、系统地观察和测度“正交生命”和“人造生命”,一系列的元件库、设计工具、自动化装备已经得到开发,不少专利已嵌入其中,与软件著作权等其他知识产权共同为合成生物学领域“基础设施”的发展提供权利保障。
近年来,“细胞工厂”和“无细胞体系”等交叉前沿受到广泛关注。由于“细胞工厂”和“无细胞体系”开发利用大多涉及天然产物、功能蛋白等成分的表达,表达系统的应用场景涉及到温度、养分等诸多环境条件,不同类型的底盘细胞和无细胞体系的应用对象和场景也有较大的差异,技术研发涉及元件和器件的集成、异源合成和调控,对元件的内禀参数等要求也较高,这些复杂要素和条件意味着需要多角度的协同考虑。从目前的专利布局来看,这方面的融合技术开发仍处于早期发展阶段。同时,半导体合成生物学、数字细胞等领域未来发展空间较大,而这些技术的专利保护要件众多,相关的知识产权共享机制和惠益分配机制的建立,需要深入探讨。
3.2 标准必要专利界定和使用,支持开源与共享
合成生物学的核心思想是基于标准化的生物元件设计新的生物功能。通过标准化,设计和改造生物系统所需的生物元件得以界定,其功能得以刻画和抽象化,而元件的储存和组装、适配等问题,最好的解决方案也是建立标准。因而,合成生物学的发展必然绕不开标准的制定、“标准必要专利”的界定。信息技术领域的发展,已经为“标准必要专利”的界定和使用提供了参考:在标准化的基础上实现从“1.0”到“2.0”再到“N.0”版本的升级,或许是可供参考的策略。不过,生物技术也有其不同于信息技术之处(例如合成生物学相关的安全、伦理等方面的考量,与信息技术有着显著差别)。当前,对于合成生物学的“标准必要专利”界定和使用的探讨仍然较少,然而随着专利布局的日渐增多,合成生物学相关标准的增值问题、开源共享与专利保护等问题或将成为合成生物学领域发展的重要课题。
3.3 加强知识产权管理,促进产品准入和应用
对于生物技术的系统性和标准化,生物线路等开发非常重要。生物线路的创造涉及单个生物元件和元件的逻辑组合,这两方面的技术都与线路相关的专利保护密切相关。同时,生物线路设计的价值,最终体现在“底盘细胞”体系及其表达的最终产物中。因而,加强生物线路等相关技术的专利布局,至少体现在元件、线路构建、底盘细胞适配、终产物的价值这四方面。对这些要素的合理组配,是构成生物线路相关专利的价值评估的基本要件。
另外,合成生物学产品的准入,也与专利等知识产权管理密切相关,知识产权体系在合成生物学“管”和“促”的协同中发挥着支点作用。从某种程度上看,合成生物学知识产权体系和标准体系的建立是“一体两面”,同时还在合成生物学的技术研发、产品准入和应用开发中发挥着转化与调控节点的作用。其具体的节点功能,又表现在知识产权体系中的专利保护、标准体系中的产品准入标准两方面,建立与之相匹配的、量身定制的管理架构,将进一步促进合成生物学时代的技术开发、社会治理、产业发展。
参考文献
开启生命科学"会聚"研究新时代
[J].
Synthetic biology: unsealing the convergence era of life science research
[J].
A brief history of synthetic biology
[J].
Engineering a mevalonate pathway in Escherichia coli for production of terpenoids
[J].
2018 Semiconductor synthetic biology roadmap
[R/OL].
Durham, NC, UK: Semiconductor Research Corporation
创新政策体系,保障合成生物学科技与产业发展,中国科学院院刊,2018,33(11):1260-1267.LIU X, ZENG Y, WANG L W,
. Innovative policy system to ensure the development of synthetic biology
[J].