|
||
|
中药药效成分群的合成生物学研究进展
合成生物学
2024, 5 (3):
631-657.
DOI:10.12211/2096-8280.2023-082
中药是中华民族的文化瑰宝,也是我国在新药创制领域的重要驱动力。许多中药材来源于稀缺物种,其药效物质的规模化获取困难,是制约中药新药创制研究的重要瓶颈。合成生物学的出现和快速发展为解决这一瓶颈问题提供了新的途径。目前,中药药效物质的合成生物学研究在单个药效分子的生物制备方法上取得了重要进展。中药的药效主要源于多成分作用的叠加和协同,所以药效成分群是中药药效物质的主要形式,然而针对药效成分群的合成生物学研究鲜有报道。建立中药药效成分群合成生物技术的关键是精确调控组成分子的比例,从而产出优质药效成分群。本文首先总结了挥发油、总皂苷、总黄酮、总木脂素、总生物碱等重要类型中药药效成分群形成机制的研究进展。然后,重点以檀香挥发油为例,介绍如何通过酶工程和代谢工程的联合运用实现药效成分群成分比例和产量的双重优化。最后,对中药药效成分群合成生物学领域的未来研究重点进行了展望,包括:(1)加强中药药效成分群生物合成途径解析方面的研究,重点深入阐明复杂药效成分群的形成机制;(2)加强代谢优化手段方面的创新研究,重点揭示未知代谢调控机制并基于此发展创新调控策略;(3)加强酶工程方法学的创新研究,重点发展新型理性设计和定向进化的联用技术以及人工智能辅助的酶工程技术。 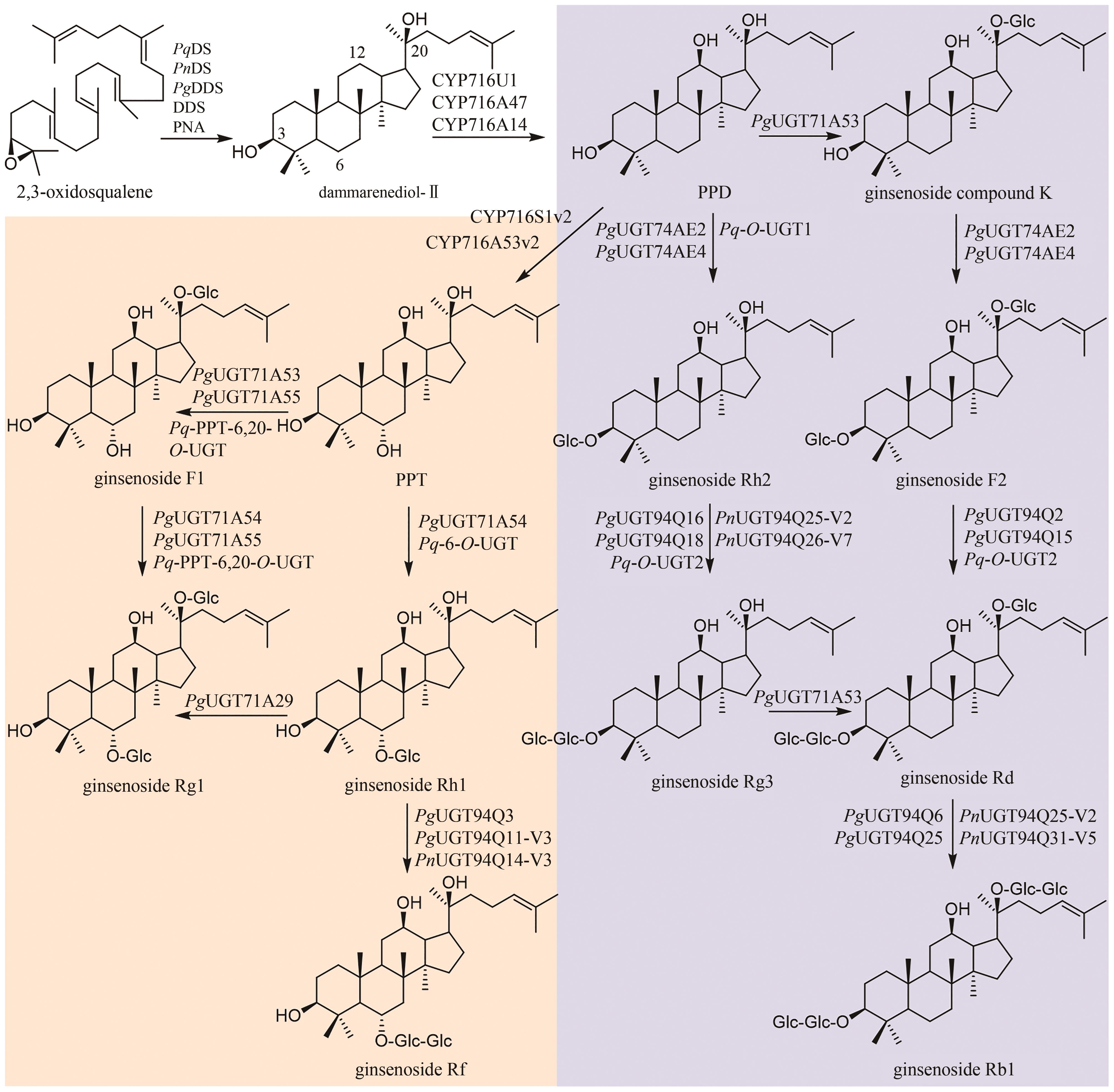 View image in article
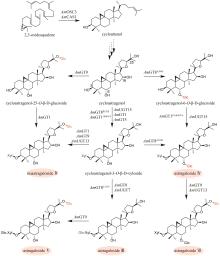
图3
人参皂苷类成分群的生物合成途径
正文中引用本图/表的段落
国内外学者对人参皂苷的生物合成进行了深入的研究(图3)。首先,达玛烯二醇-Ⅱ合酶(DS)环化2,3-环氧鲨烯,生成达玛烯二醇(dammarenediol-Ⅱ)。目前,已鉴定多个DS酶,如:人参(Panax ginseng C. A. Mey.)中的PNA[58]、DDS[59]和PgDDS[60]以及三七[Panax notoginseng (Burk.) F. H. Chen]中的PnDS[61]和西洋参(Panax quinquefolium L.)中的PqDS[62]。人参中的三个CYP酶CYP716U1、CYP716A47和CYP716A14负责催化达玛烯二醇C12位的羟基化,生成PPD;然后,CYP716S1v2和CYP716A53v2催化C6位羟基化,生成PPT(图3)[63-65]。
人参皂苷生物合成的糖基化过程十分复杂,同一步骤往往可被数种甚至几十种糖基转移酶催化,而一种糖基转移酶也常常可以接受多个底物或者催化不同位点的糖基化。因此,对于每步糖基化反应,这里仅列举催化效率较高的糖基转移酶。PPD通过两条途径生成人参皂苷Rd(图3)。在第一条途径中,PPD可在PgUGT71A53和PgUGT74AE2/PgUGT74AE4的连续催化下,发生C20位和C3位羟基的糖基化,生成人参皂苷F2;之后,在PgUGT94Q2/PgUGT94Q15/Pq-O-UGT2的催化下,C3位糖链被进一步延长,得到人参皂苷Rd[66-68]。在第二条途径中,PgUGT74AE2/PgUGT74AE4/Pq-O-UGT1催化PPD的C3位羟基的糖基化,生成人参皂苷Rh2[66,68-70];进一步在PgUGT94Q16/PgUGT94Q18/PnUGT94Q25-V2/PnUGT94Q26-V7/Pq-O-UGT2的催化下,延长C3位糖链,生成人参皂苷Rg3[66-69];最后,PgUGT71A53糖基化人参皂苷Rg3的C20位羟基,生成人参皂苷Rd[71]。人参皂苷Rd在PgUGT94Q6/PgUGT94Q25/PnUGT94Q25-V2/PnUGT94Q31-V5的催化下,延长C20位糖链,得到人参皂苷Rb1[71]。
从PPT到人参皂苷Rg1的转化也有两条途径(图3)。在第一条途径中,PgUGT71A53/PgUGT71A55/Pq-PPT-6,20-O-UGT催化PPT的C20位羟基糖基化,生成人参皂苷F1[71-73];随后,PgUGT71A54/PgUGT71A55/Pq-PPT-6,20-O-UGT糖基化人参皂苷F1的C6位羟基,得到人参皂苷Rg1[72]。在第二条途径中,PgUGT71A54/Pq-6-O-UGT催化PPT的C6位羟基糖基化,生成人参皂苷Rh1;进一步在PgUGT71A29的催化下,发生C20位羟基糖基化,生成人参皂苷Rg1[74]。此外,人参皂苷Rh1还可在PgUGT94Q3/PgUGT94Q11-V3/PnUGT94Q14-V3的催化下,发生C6位糖基化,生成人参皂苷Rf[68](图3)。
本文的其它图/表
|