|
||
|
高黏性蛋白材料的合成生物学及应用
合成生物学
2025, 6 (4):
806-828.
DOI:10.12211/2096-8280.2025-043
高黏性蛋白材料因其卓越的生物黏附性和潜在的生物相容性,在生物医用材料和黏合剂领域展现出巨大的应用潜力。然而,传统方式获取的高黏蛋白材料面临诸多挑战,如产量低、结构复杂、难以规模化生产等。合成生物学作为新兴的交叉学科,为解决这些瓶颈提供了创新策略。本综述系统总结了近年来高黏性蛋白材料的生物合成、改性及应用进展,重点突出了合成生物学在解决高黏性蛋白材料产量、可控性以及功能多样性等方面的优势。全面梳理了基因工程实现对贻贝黏蛋白、藤壶胶蛋白和扇贝足丝蛋白等黏附蛋白的精确设计和高效表达,从而克服高黏蛋白材料在产量和可控性方面的限制。同时,综述了这些蛋白材料在生物黏合剂和医用功能涂层方面的独特优势,如贻贝蛋白的湿面黏附性、藤壶胶蛋白的强黏附性以及类弹性蛋白的可调控性。通过合成生物学方法,可以突破高黏蛋白材料在产量、性能和功能方面的限制,加速其在组织工程、表界面改性等领域的应用。最后,总结了当前合成生物学在高黏蛋白材料领域的最新进展和创新点,并展望了其未来的发展方向,为开发高性能、多功能的高黏蛋白材料提供了新的思路和策略。  View image in article
图3
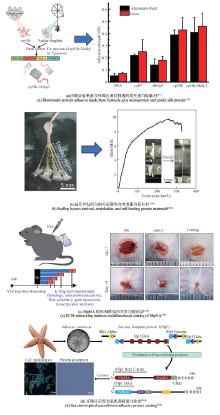
基于Mfp的医用材料
正文中引用本图/表的段落
Mfp凭借其优异的黏附能力和生物相容性在生物医学领域也发挥着重要作用。通过旋涂、浸涂等方法使Mfp在医用材料表面形成涂层,从而改善细胞的黏附、增殖和分化等行为[87]。此外,Mfp还可作为介质材料,将细胞微环境因子、核酸、治疗药物、无机纳米粒子等生物分子固定在靶表面上[88]。然而,由于天然黏性蛋白或重组黏性蛋白组分单一、机械性能不理想,因此,通过设计功能肽或其他重组蛋白与Mfp的融合来实现的复合型黏合材料应运而生。例如,Kin等[89]将抗菌肽(AMP)与Mfp融合,以克服AMP稳定性和毒性限制。研究表明,该融合蛋白是一种具有新型抗菌活性的、热稳定且安全的革兰氏阴性菌抑制剂。此外,Hu等[90]基于聚乙烯吡咯烷酮(PVP)-聚乙二醇丙烯酸酯(PEGDA)的化学交联网络和Mfp-5的物理网络,开发了一种双网络水凝胶涂层(PPM)。得益于Mfp-5的仿生黏附特性和抗菌活性,PPM表现出优异的抗菌能力和超润滑性能[图3(a)]。类似地,Lee等[91]基于Mfp与丝素蛋白(SF)构建了双面电纺纳米纤维止血敷料:内侧含DOPA的Mfp层通过氢键、金属配位等激活血小板并增强凝血,同时提供湿态组织黏附;外侧由于SF的表面特性转换,保护伤口部位免受意外黏附以及包括细菌在内的污染物的渗透。实验验证表明,这种局部多功能双面纳米纤维止血敷料基于两种生物相容性和可生物降解的蛋白质生物材料,在内出血护理应用中具有良好的应用前景[图3(b)]。Cheong等[92]将Mfp与细胞外基质(ECM)中的生物功能肽相结合,通过增强细胞黏附、增殖、神经分化和神经突形成,加速神经再生。为了促进神经和雪旺细胞的接触引导,将Mfp与合成聚合物聚乳酸-羟基乙酸(PLGA)结合,制成电纺对齐纳米纤维导管,以控制溶解度和机械性能。体外和体内实验表明,Mfp的黏附性、ECM肽的整合素介导相互作用以及对齐纳米纤维的接触引导的多维策略协同加速了功能性神经再生。这种基于Mfp的多维方法为神经再生应用(包括神经移植)提供了新的机遇[图3(c)]。
本文的其它图/表
|