|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Research Progress in Plant-Derived Vaccines
Synthetic Biology Journal
DOI: 10.12211/2096-8280.2025-029
Table 1
Plant-derived foreign substances that have been put into clinical or animal experiments and their expression methods
Extracts from the Article
此外,一些植物源疫苗已经获得了监管机构的批准,并开始商业化生产和分发。例如一种通过烟草植株生产的埃博拉病毒疫苗在2019年获得了欧洲药品管理局的批准[24]。除此之外还有许多用烟草生产的针对Covid-19的疫苗项目,例如2021年就投入临床的SARS-CoV-2 VLP Vaccine (IBIO-200)以及SARS-CoV-2 Subunit Vaccine (IBIO-201)项目[25],与之同时的还有投入Ⅲ期临床试验的SARS-CoV-2 Spike protein项目等[26, 27](表1)。
抗原是指能够刺激机体免疫系统产生免疫应答,并能与免疫应答产物(抗体或致敏淋巴细胞)在体内外发生特异性反应的物质。植物能够高效表达病原体表面蛋白等抗原,为疫苗开发提供了新的平台。研究表明,通过植物表达系统,能够生产具有良好免疫原性的抗原。任兆钧等利用烟草TMV-30B外源蛋白高效表达载体,将口蹄疫毒株的免疫抗原克隆并表达于烟草叶片,该研究中提到的免疫抗原是猪O型口蹄疫病毒(FMDV)抗原表位融合结构蛋白VP1,是口蹄疫病毒的主要免疫原性蛋白,它包含了病毒的抗原表位,能够刺激机体产生免疫应答[46]。早在1999年,Buetow等就在烟草中开发了针对呼吸道合胞病毒(RSV)的植物源疫苗。RSV F蛋白由一个50 kDa的羧基末端F1片段和一个20kDa的氨基末端F2片段组成, 该二聚体的109和136氨基酸残基后存在两个furin蛋白酶切位点,酶切后将暴露F1氨基末端的疏水融合肽,使该抗原更容易被免疫细胞识别并结合[47]。同年十月,Langridge等将编码霍乱毒素B亚基(CTB)基因插入植物表达载体,成功诱导小鼠产生与天然CTB相同的免疫反应[48]。Sohrab等在2020年开发的可食用疫苗能够有效表达中东呼吸综合征冠状病毒刺突蛋白S1亚基的抗原, S1亚基包括N端结构域(NTD)和C端结构域(CTD),其中CTD也被称为受体结合结构域(RBD),负责与宿主细胞的受体结合[49](表2)。
病毒样颗粒(Virus-like particles,VLPs)是一种由病毒结构蛋白自行装配而成的蛋白质颗粒。它们在形态结构上与天然的病毒颗粒相似,因此具有很强的免疫原性和生物学活性,且不含病毒核酸,没有复制能力,也不具有感染性,因此病毒样颗粒疫苗安全性较高。王跃驹于2019年利用生菜作为表达平台,成功生产病毒样颗粒的乙肝VLP疫苗,接种新西兰白兔后白兔产生免疫,并通过ELISA和假病毒颗粒中和试验验证了其生物活性[50],发现乙型肝炎病毒核心蛋白HBcAg会在体外自组装形成二十面体对称结构,这种结构与天然乙肝病毒微粒的构象近似,直径约为30 nm,呈现较为均一的球形,外源序列重复且高密度地展示在VLPs的表面,这使得VLPs进入机体后能够快速诱导机体产生针对外源性抗原的特异性体液免疫及细胞免疫应答,具有极强的免疫原性与生物活性[51];在2020年,他又利用相同技术成功表达了具有生物活性的HPV疫苗,该研究中产生的VLPs具有二十面体对称结构,这是类似于野生型VLPs的形态[28]。与之结构类似的还有Rybicki于2016年在植物细胞利用农杆菌转化法中成功稳定表达的HPV假病毒粒子,而该VLP疫苗已经进行了中和测定试验[33]。同样的技术还于2021年用于植物源牛瘤病毒(BPV)病毒样颗粒和假病毒粒子的生产,BPV VLPs能够诱导产生针对BPV的特异性抗体,包括IgG和中和(VN)抗体,以及促进Th1和Th2细胞因子的分泌,如IL-2、IL-4和IFN-γ[34]。猪细小病毒(PPV)导致母猪繁殖失败, CHO等人在2023年用本氏烟草成功表达可以让猪抵御PPV的PPV 1 -82 VP 2蛋白,这些蛋白自组装成的VLPs的直径范围在22.3到25.7纳米之间,在对怀孕母猪的抗病实验中,接种了PPV1-82 VP2的母猪在感染PPV株后,成功诱导了免疫反应并产下正常胎儿,而未接种疫苗的母猪则流产[52],这些结果表明, PPV1-82 VP2 VLP疫苗在结构和功能上都显示出了作为有效疫苗候选物的潜力(表3)。
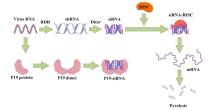
通过将疫苗抗原表达在植物中,然后将植物材料制成口服疫苗,可以实现更方便、更广泛的疫苗接种。虽然口服疫苗的研发仍面临一些挑战,但其潜力巨大。张玉满等发明了一种利用枸杞作为TMV瞬时表达外源蛋白的生物反应器并成功表达了GFP外源报告基因,可将该体系利用于口服疫苗的研发与生产[68]。幽门螺旋杆菌ureB抗原基因被Gu等人克隆到pCAMBIA1301质粒中,位于CaMV35S启动子和八氨酸合酶(OCS)终止子之间的gus(β-葡萄糖苷酶)报告基因的5'端,通过农杆菌介导的转化将其导入水稻基因组。水稻可用于口服疫苗的研发,RT-PCR和Western blot分析也验证了水稻植物中ureB基因的表达。这些结果为进一步研究可食用转基因水稻在幽门螺旋杆菌疫苗的研发奠定了基础[41]。ZHANG等人还报道了一种有助于治疗乙型肝炎病毒(HBV)感染的转基因生菜。他们设计了两种针对HBV表面抗原(HBsAg)的人工miRNA(amiR471和amiR519),并在稳定的转基因生菜品种中单独表达,将这些生菜喂食小鼠,使小鼠产生积极免疫反应[69]。Wang等利用农杆菌介导的转化方法生成了表达日本脑炎病毒(JEV)包膜蛋白(E)的转基因水稻,该基因在双花椰菜花纹病毒(CaMV 35S)启动子的调控下进行表达,在叶片中的表达水平为每毫克总可溶性蛋白1.1-1.9微克。对小鼠进行转基因水稻植物蛋白提取物的口服免疫后,能够检测到针对E蛋白的黏膜免疫反应[38]。
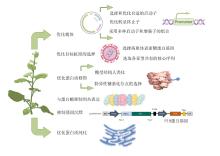
稳定表达系统是指将目标抗原基因稳定地导入植物基因组中,使其在世代间持续表达[86]。目前应用最广泛的是稳定核表达和稳定叶绿体表达,而稳定核表达主要是农杆菌介导转化法,稳定叶绿体表达主要使用基因枪和显微注射法[87]。Danniell等于2007年提供了哺乳动物对感染性病原体免疫力疫苗的方案,其用到了叶绿体这种质体转化以产生保护性抗原的载体,并成功表达药物蛋白[88]。叶绿体表达系统会丧失真核表达系统部分翻译后修饰方面的优势,比如糖基化、泛素化和磷酸化等,这些修饰可能影响蛋白的功能、定位、稳定性及与其他分子的相互作用,但叶绿体表达系统也具有自身的修饰能力,可进行一些基本的翻译后修饰过程,如二硫键形成、脂化和磷酸化等,能够满足部分蛋白的正确折叠和功能需求[89]。叶绿体表达系统适合生产亚单位疫苗如针对骨髓灰质炎病毒的加强型疫苗 CTB-VP1,VP1 属于病毒衣壳蛋白,其在烟草叶绿体中的表达具有免疫效果好、生产成本低等优势。还有霍乱毒素 B 亚基、人胰岛素原的融合蛋白等,其表达量高,且通过注射能展现出相应的功效[90]。某些病毒样颗粒的组装也不依赖糖基化修饰,因此可以使用叶绿体表达系统进行研发,如中国农业科学院生物技术研究所沈桂芳教授的叶绿体基因工程实验室在烟草叶绿体中成功表达的口蹄疫病毒主要抗原VP1基因、猪瘟病毒主要抗原 E2 基因等动物植物疫苗抗原[90]。而对于一些需要复杂糖基化修饰才能具有正确抗原性和免疫原性的疫苗抗原,叶绿体表达系统无法满足其修饰需求,导致表达的抗原活性低或无活性,如某些流感病毒疫苗抗原等,核表达系统更适合此类疫苗的生产[81],此外,叶绿体中的蛋白可能面临不同的降解风险,对于一些对稳定性要求极高、在叶绿体中易被降解的疫苗蛋白,核表达系统可通过内质网等细胞器为蛋白提供更稳定的折叠和保护环境,减少蛋白降解,更具优势[89]。常见的表达载体有Gateway、p1303、P33cym11、pBI 121、pBI 221等[91],常用的植物宿主表达器官一般为作物种子胚乳,如Matsumoto等用水稻胚乳稳定表达抗轮虫Ascaris suum的保护性抗原As16。该抗原作为与霍乱毒素B亚单位(CTB)融合的嵌合蛋白,其在胚乳中的表达水平达到了每克种子50微克。将转基因(Tg)水稻种子结合霍乱毒素(CT)作为粘膜佐剂喂给小鼠后成功诱导了特异性抗原As16的血清抗体反应。这表明,水稻稳定遗传转化递送的抗原作为一种预防性可食用疫苗,可以控制动物的寄生虫感染[42]。Yoshida等将针对阿尔茨海默病(AD)的Aβ 42基因与绿色荧光蛋白基因融合后,采用农杆菌法转入水稻中。当转基因的水稻被口服给小鼠时,血清中的抗Aβ抗体滴度明显上升。当小鼠被喂食煮熟的转基因水稻时,观察到了相同的结果。这些结果表明,使用水稻稳定表达的可食用疫苗对治疗阿尔茨海默病是可行的[45]。Nochi等开发了一种基于水稻稳定表达的口服疫苗,该疫苗表达霍乱毒素B亚单位(CTB),其表达受特定于胚乳的表达启动子2.3-kb谷蛋白GluB-1控制,并经过密码子优化以便在大米种子中表达,且每颗种子的胚乳中平均存储了30微克的CTB,当以粘膜方式喂食时,表达CTB的种子被M细胞吸收,成功诱导产生具有中和活性的CTB特异性血清IgG和粘膜IgA抗体[92]。这些基于水稻稳定遗传转化的疫苗为大规模口服接种人群提供了一种高度实用和具有成本效益的策略以应对感染[93]。Suzuki等测试了新开发的亚单位疫苗对支气管哮喘进行口服免疫治疗的可行性,该疫苗中包含了螨虫过敏原(Der p 1)的一个片段(p45-145),这个片段被包裹在转基因(Tg)水稻种子的内质网源性蛋白体中,且接种后明显降低了过敏原特异性IgE和IgG的血清水平,因此这种疫苗不会引起非特异性抑制,这在许多口服耐受方案中是一个突破。结果表明,基于水稻稳定表达的新疫苗策略是针对包括支气管哮喘在内的过敏疾病的过敏原特异性口服免疫治疗的一个有前途的方法[94]。而Yang表达一种房尘螨(HDM)过敏源Der p 1,C端带KDEL标签的Der p 1过敏源在胚乳特异性的GluB1启动子的控制下,特定积累在种子胚乳组织中,Der p 1在每粒种子中达到了最大浓度58微克,存放在内质网(ER)来源的蛋白体I(PB-I)中。结果表明,稳定转基因Der p 1水稻种子是治疗HDM过敏的安全潜在口服疫苗[43]。基因枪转化法又叫粒子轰击法,将DNA吸附在直径几微米的金粉或者钨粉上,然后将微粒高速打入外植体,高速微粒可以穿透植物细胞的细胞壁,微粒进入细胞后,吸附的DNA也从微粒中解离出来并在植物细胞中表达[95],如唐琳等用高压氦气式基因枪成功将外源基因导入番红花愈伤组织[96],张馨悦使用基因枪转化了萱草的花粉[97]。由于农杆菌转化法拥有更稳定高效的特性,所以在植物源疫苗研发生产的过程中,基因枪的使用概率并不高[95]。
在遗传转化后的植物培养过程中,需要对基因工程转入的抗性基因用相应的抗生素进行筛选培养以及分化培养,转化成功的植物可以是温室或田间,还需要根据不同植物以及不同生长情况给予激素或肥料以促进其生长,在从而增加生长过程中目标抗原蛋白的产量。在用水稻愈伤组织进行遗传转化后,共培养时考虑农杆菌和水稻细胞的活性,因此需要在25℃暗箱培养2-3天,而筛选阶段则需要将温度控制在28-32 ℃,不同的筛选和分化条件也决定了后续光周期的供给时间[98]。烟草的幼嫩叶片、茎段和带有叶片的茎段作为稳定转化的最常用的外植体,在MS+0.1mg/L 6-BA+0.5mg/L NAA的培养基中能诱导形成不定芽和根,在MS+0.5 mg/L 6-BA+0.1 mg/L NAA的培养基和MS+0.5 mg/L 6-BA+0.5 mg/L NAA的培养基中能脱分化形成愈伤组织[99]。瞬时表达系统对于培养条件的要求更简洁,不需要频繁更换,如烟草对光照强度的需求仅需考虑两个不同的生长阶段,烤烟苗期的光饱和点在1-2万Lx(178.6 μmol·m-2·s-1-357.1 μmol·m-2·s-1),大田期在3~5万Lx(535.7 μmol·m-2·s-1-892.9 μmol·m-2·s-1),光照周期16h/d,以及日夜温度控制在28/21℃时最有利于烟草植株的生长以及蛋白的表达[100, 101]。
在植物源疫苗的开发中,选择合适的表达载体是至关重要的。如质粒、病毒或其他表达系统,并且需要考虑不同载体的复制能力、稳定性、毒性、毒性基因的缺失等因素。关于表达载体选择的考虑因素如复制能力,即选择能够在植物细胞中高效复制的载体,以确保高水平的基因表达,在研发过程中,也可以使用植物生长调节剂调节复制和表达效率[108]。例如,2012年Rosenthal等构建了经修饰的基于菜豆黄矮病毒(BeYDV)的载体,该载体被设计为允许多个重组基因的共表达,从而提供了快速且成本效益高的大规模生产重组蛋白用于医药和工业的载体工具[109]。LAI等使用菜豆黄矮病毒的双生病毒复制子系统构建了新型载体,成功在莴苣中高水平表达诺瓦病毒VLP和针对埃博拉病毒和西尼罗河病毒的治疗性单克隆抗体mAb[29],喻文聪等使用PCR对BjuA03.TTG2基因上游启动子序列片段进行特异性扩增并构建到pCAMBIA1304植物表达载体中,促进了下游目的片段的表达[110]。不同载体的选择会直接影响到疫苗基因的表达效率和稳定性,选择能够在植物体内稳定存在的载体,避免基因丢失或突变,还要确保所选载体对宿主植物无毒性,不会影响植物的生长和发育,此外还需要考虑避免毒性基因的缺失造成的影响,譬如从载体中去除任何可能对人类或动物有害的毒性基因,确保疫苗的安全性。Takita等开发了一种新的二元质粒(pTACAtg 1),在克隆位点的两侧携带长的基因组DNA片段。将花椰菜花叶病毒35 S启动子:β-葡萄糖醛酸酶(35 S:GUS)基因克隆到pTACAtg 1中,并将其与pTACAtg 1上的长侧翼序列一起导入植物中。在分离的转基因植株中,拷贝数减少,检测到的GUS表达比那些携带插入没有侧翼区的对照植株更稳定。在他们的研究结果中,转基因拷贝数的减少抑制了其基因表达的变异和沉默,因此pTACAtg 1载体将适用于稳定转化体的产生和转基因的表达分析[111]。
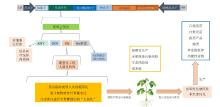
植物源疫苗的分类主要基于表达的不同重组蛋白类型以及生产和给药方式.这些疫苗可以表达特定病原体的抗原或病毒样颗粒(VLP),也可以根据给药途径设计为注射疫苗或口服疫苗,植物源疫苗具有生产成本低、易于大规模生产、便于储存和分发的优势,同时能够有效诱导粘膜免疫,此外,疫苗也可以根据不同宿主植物(如烟草、小麦、马铃薯、水稻等)进行分类,以优化其生产和应用效果. ... Merck's ERVEBO? 1 ... 此外,一些植物源疫苗已经获得了监管机构的批准,并开始商业化生产和分发.例如一种通过烟草植株生产的埃博拉病毒疫苗在2019年获得了欧洲药品管理局的批准[ Plant-Based COVID-19 Vaccines: Current Status, Design, and Development Strategies of Candidate Vaccines 1 2021 ... 此外,一些植物源疫苗已经获得了监管机构的批准,并开始商业化生产和分发.例如一种通过烟草植株生产的埃博拉病毒疫苗在2019年获得了欧洲药品管理局的批准[ Phase 1 randomized trial of a plant-derived virus-like particle vaccine for COVID-19 1 2021 ... 此外,一些植物源疫苗已经获得了监管机构的批准,并开始商业化生产和分发.例如一种通过烟草植株生产的埃博拉病毒疫苗在2019年获得了欧洲药品管理局的批准[ Plant-made vaccines against viral diseases in humans and farm animals 1 2023 ... 此外,一些植物源疫苗已经获得了监管机构的批准,并开始商业化生产和分发.例如一种通过烟草植株生产的埃博拉病毒疫苗在2019年获得了欧洲药品管理局的批准[ 生菜作为宿主在表达人乳头瘤病毒蛋白或制备人宫颈癌疫苗中的应用 2 ... Plant-derived foreign substances that have been put into clinical or animal experiments and their expression methods
病毒样颗粒(Virus-like particles,VLPs)是一种由病毒结构蛋白自行装配而成的蛋白质颗粒.它们在形态结构上与天然的病毒颗粒相似,因此具有很强的免疫原性和生物学活性,且不含病毒核酸,没有复制能力,也不具有感染性,因此病毒样颗粒疫苗安全性较高.王跃驹于2019年利用生菜作为表达平台,成功生产病毒样颗粒的乙肝VLP疫苗,接种新西兰白兔后白兔产生免疫,并通过ELISA和假病毒颗粒中和试验验证了其生物活性[ Tobacco-Expressed FMD Plant Genetic Engineering Vaccine and Its Preparation Method 2 ... 抗原是指能够刺激机体免疫系统产生免疫应答,并能与免疫应答产物(抗体或致敏淋巴细胞)在体内外发生特异性反应的物质.植物能够高效表达病原体表面蛋白等抗原,为疫苗开发提供了新的平台.研究表明,通过植物表达系统,能够生产具有良好免疫原性的抗原.任兆钧等利用烟草TMV-30B外源蛋白高效表达载体,将口蹄疫毒株的免疫抗原克隆并表达于烟草叶片,该研究中提到的免疫抗原是猪O型口蹄疫病毒(FMDV)抗原表位融合结构蛋白VP1,是口蹄疫病毒的主要免疫原性蛋白,它包含了病毒的抗原表位,能够刺激机体产生免疫应答[
病毒样颗粒(Virus-like particles,VLPs)是一种由病毒结构蛋白自行装配而成的蛋白质颗粒.它们在形态结构上与天然的病毒颗粒相似,因此具有很强的免疫原性和生物学活性,且不含病毒核酸,没有复制能力,也不具有感染性,因此病毒样颗粒疫苗安全性较高.王跃驹于2019年利用生菜作为表达平台,成功生产病毒样颗粒的乙肝VLP疫苗,接种新西兰白兔后白兔产生免疫,并通过ELISA和假病毒颗粒中和试验验证了其生物活性[ Plant-derived vaccines against respiratory syncytial virus 3 ... 抗原是指能够刺激机体免疫系统产生免疫应答,并能与免疫应答产物(抗体或致敏淋巴细胞)在体内外发生特异性反应的物质.植物能够高效表达病原体表面蛋白等抗原,为疫苗开发提供了新的平台.研究表明,通过植物表达系统,能够生产具有良好免疫原性的抗原.任兆钧等利用烟草TMV-30B外源蛋白高效表达载体,将口蹄疫毒株的免疫抗原克隆并表达于烟草叶片,该研究中提到的免疫抗原是猪O型口蹄疫病毒(FMDV)抗原表位融合结构蛋白VP1,是口蹄疫病毒的主要免疫原性蛋白,它包含了病毒的抗原表位,能够刺激机体产生免疫应答[
病毒样颗粒(Virus-like particles,VLPs)是一种由病毒结构蛋白自行装配而成的蛋白质颗粒.它们在形态结构上与天然的病毒颗粒相似,因此具有很强的免疫原性和生物学活性,且不含病毒核酸,没有复制能力,也不具有感染性,因此病毒样颗粒疫苗安全性较高.王跃驹于2019年利用生菜作为表达平台,成功生产病毒样颗粒的乙肝VLP疫苗,接种新西兰白兔后白兔产生免疫,并通过ELISA和假病毒颗粒中和试验验证了其生物活性[
病毒样颗粒(Virus-like particles,VLPs)是一种由病毒结构蛋白自行装配而成的蛋白质颗粒.它们在形态结构上与天然的病毒颗粒相似,因此具有很强的免疫原性和生物学活性,且不含病毒核酸,没有复制能力,也不具有感染性,因此病毒样颗粒疫苗安全性较高.王跃驹于2019年利用生菜作为表达平台,成功生产病毒样颗粒的乙肝VLP疫苗,接种新西兰白兔后白兔产生免疫,并通过ELISA和假病毒颗粒中和试验验证了其生物活性[ Development Of An Edible Vaccine 2 ... 抗原是指能够刺激机体免疫系统产生免疫应答,并能与免疫应答产物(抗体或致敏淋巴细胞)在体内外发生特异性反应的物质.植物能够高效表达病原体表面蛋白等抗原,为疫苗开发提供了新的平台.研究表明,通过植物表达系统,能够生产具有良好免疫原性的抗原.任兆钧等利用烟草TMV-30B外源蛋白高效表达载体,将口蹄疫毒株的免疫抗原克隆并表达于烟草叶片,该研究中提到的免疫抗原是猪O型口蹄疫病毒(FMDV)抗原表位融合结构蛋白VP1,是口蹄疫病毒的主要免疫原性蛋白,它包含了病毒的抗原表位,能够刺激机体产生免疫应答[
病毒样颗粒(Virus-like particles,VLPs)是一种由病毒结构蛋白自行装配而成的蛋白质颗粒.它们在形态结构上与天然的病毒颗粒相似,因此具有很强的免疫原性和生物学活性,且不含病毒核酸,没有复制能力,也不具有感染性,因此病毒样颗粒疫苗安全性较高.王跃驹于2019年利用生菜作为表达平台,成功生产病毒样颗粒的乙肝VLP疫苗,接种新西兰白兔后白兔产生免疫,并通过ELISA和假病毒颗粒中和试验验证了其生物活性[ 生菜作为宿主在表达乙肝疫苗中的应用 1 ... 病毒样颗粒(Virus-like particles,VLPs)是一种由病毒结构蛋白自行装配而成的蛋白质颗粒.它们在形态结构上与天然的病毒颗粒相似,因此具有很强的免疫原性和生物学活性,且不含病毒核酸,没有复制能力,也不具有感染性,因此病毒样颗粒疫苗安全性较高.王跃驹于2019年利用生菜作为表达平台,成功生产病毒样颗粒的乙肝VLP疫苗,接种新西兰白兔后白兔产生免疫,并通过ELISA和假病毒颗粒中和试验验证了其生物活性[ Application of Lettuce as a Host in Expressing Hepatitis B Vaccine 1 ... 病毒样颗粒(Virus-like particles,VLPs)是一种由病毒结构蛋白自行装配而成的蛋白质颗粒.它们在形态结构上与天然的病毒颗粒相似,因此具有很强的免疫原性和生物学活性,且不含病毒核酸,没有复制能力,也不具有感染性,因此病毒样颗粒疫苗安全性较高.王跃驹于2019年利用生菜作为表达平台,成功生产病毒样颗粒的乙肝VLP疫苗,接种新西兰白兔后白兔产生免疫,并通过ELISA和假病毒颗粒中和试验验证了其生物活性[ 具备定点偶联功能的HBc-VLPs的制备与性质鉴定 1 2020 ... 病毒样颗粒(Virus-like particles,VLPs)是一种由病毒结构蛋白自行装配而成的蛋白质颗粒.它们在形态结构上与天然的病毒颗粒相似,因此具有很强的免疫原性和生物学活性,且不含病毒核酸,没有复制能力,也不具有感染性,因此病毒样颗粒疫苗安全性较高.王跃驹于2019年利用生菜作为表达平台,成功生产病毒样颗粒的乙肝VLP疫苗,接种新西兰白兔后白兔产生免疫,并通过ELISA和假病毒颗粒中和试验验证了其生物活性[ Preparation and Characterization of HBc-VLPs with Site-Specific Conjugation Functionality 1 2020 ... 病毒样颗粒(Virus-like particles,VLPs)是一种由病毒结构蛋白自行装配而成的蛋白质颗粒.它们在形态结构上与天然的病毒颗粒相似,因此具有很强的免疫原性和生物学活性,且不含病毒核酸,没有复制能力,也不具有感染性,因此病毒样颗粒疫苗安全性较高.王跃驹于2019年利用生菜作为表达平台,成功生产病毒样颗粒的乙肝VLP疫苗,接种新西兰白兔后白兔产生免疫,并通过ELISA和假病毒颗粒中和试验验证了其生物活性[ A Plant-Produced Porcine Parvovirus 1-82 VP2 Subunit Vaccine Protects Pregnant Sows against Challenge with a Genetically Heterologous PPV1 Strain 1 2023 ... 病毒样颗粒(Virus-like particles,VLPs)是一种由病毒结构蛋白自行装配而成的蛋白质颗粒.它们在形态结构上与天然的病毒颗粒相似,因此具有很强的免疫原性和生物学活性,且不含病毒核酸,没有复制能力,也不具有感染性,因此病毒样颗粒疫苗安全性较高.王跃驹于2019年利用生菜作为表达平台,成功生产病毒样颗粒的乙肝VLP疫苗,接种新西兰白兔后白兔产生免疫,并通过ELISA和假病毒颗粒中和试验验证了其生物活性[ Influenza virus-like particles produced by transient expression in Nicotiana benthamiana induce a protective immune response against a lethal viral challenge in mice 1 2008 ... Examples of some plant-derived enveloped VLPs
Other Images/Table from this Article
|